- Tham gia
- 28/1/21
- Bài viết
- 82,441
- Điểm
- 113
tác giả
Đề kiểm tra học kì 2 môn hóa lớp 8 NĂM 2022 CÓ MA TRẬN + ĐÁP ÁN RẤT HAY
YOPOVN xin gửi đến quý thầy cô, các em Đề kiểm tra học kì 2 môn hóa lớp 8 NĂM 2022 CÓ MA TRẬN + ĐÁP ÁN RẤT HAY. Đây là bộ Đề kiểm tra học kì 2 môn hóa lớp 8, đề thi hóa 8 học kì 2 có đáp án...........
De thi học kì 2 môn Hóa lớp 8 có đáp an
Trắc nghiệm Hóa 8 học kì 2 có đáp an
De thi Hóa lớp 8 học kì 2 tự luận
Các dạng bài tập Hóa lớp 8 học kì 2
vi|đề thi hóa lớp 8 học kì 2 năm 2020
vi|đề thi hóa lớp 8 học kì 1 năm 2020
De kiểm tra Hóa 8 giữa học kì 2
De kiểm tra Hóa 8 học kì 2
Các đề thi Hóa 8 giữa học kì 1
Trắc nghiệm Hóa 8 học kì 2 có đáp an
De thi Hóa 8 học kì 2 trắc nghiệm
De thi Hóa 8 giữa học kì 2 có đáp án
Các dạng bài tập Hóa 8 học kì 2
De thi Hóa lớp 8 học kì 2
vi|đề thi hóa lớp 8 học kì 2 năm 2020
Tổng hợp kiến thức hóa 8 học kì 2
MA TRẬN
I. PhầnTrắc nghiệm (4 điểm)
Hãy chọn một đáp án đúng nhất trong các câu (A, B, C, D) dưới đây
Câu 1: Phản ứng nào thuộc loại phản ứng hoá hợp :
A. CaCO3 + CO2 + H2O Ca(HCO3)2 C. C + O2 t0 CO2
B. KClO3 t0 KCl + O2 D . Cả A và C đúng
Câu 2. Nguyên liệu để điều chế oxi trong phòng thí nghiệm là :
A. KClO3 B. Không khí C. KMnO4 D. Cả Avà C đúng
Câu 3 1 điểm) Hòa tan 40 g NaCl vào 120 g nước. Nồng độ phần trăm của dung dịch:
1 điểm) Hòa tan 40 g NaCl vào 120 g nước. Nồng độ phần trăm của dung dịch:
A. 6% B. 25% C. 22 % D. 50%
Câu 4:Nồng độ phần trăm của dung dịch cho ta biết số gam chất tan có trong bao nhiêu gam dung dịch.
A. 100 B. 80 C. 150 D. 90
Câu 5 : Số gam nước thu được khi cho 4.2 lít H2 tác dụng với 1.4 lit khí oxi(các khí ở đktc) là:
A.3g B.2.25g C.3.375g D.4g
Câu 6 : Phản ứng hóa học có thể dùng điều chế H2 trong công nghiệp là:
A.2H2Oà2H2+O2 B.Fe+2HClàFeCl2+H2
C.Zn+2HClàFe2Cl2+H2 D.2Al+6HClà2AlCl3+H2
Câu 7: Khi thu khí H2 vào ống nghiệm bằng cách đẩy không khí, phải để úp ống nghiệm vì khí H2
A.Tan ít trong nước B.Nặng hơn không khí
C.Nhẹ hơn không khí D.Nhiệt độ hóa lỏng thấp nhật
Câu 8 : Cho biết công thức hóa học của các oxit sau: SO3, CO2, P2O5, Fe2O3, CaO.
A. Cả 5 oxit trên đều là oxit axit B.Cả 5 oxit trên đều là oxit bazzo
C.Cả 5 oxit trên đều là oxit trung tính D.5 oxit trên có cả oxit axit và oxit bazơ
Câu 9 : Cho phản ứng hóa học: 3H2 + Fe2O3 à 2Fe + 3H2O. phản ứng trên thuộc loại :
A .Phản ứng trao đổi B. Phản ứng oxi hóa – khử
C. Phản ứng hóa hợp D.Phản ứng phân hủy
Câu 10: Phân hủy hết 24,5 g KClO3 thu được thể tích O2 (đktc) là:
A.4.48 lt B.6.72 l C.22.4 l D.11.2 l
Câu 11: Phản ứng nào thuộc loại phản ứng phân hủy:
A. CaCO3 + CO2 + H2O Ca(HCO3)2 C. C + O2 t0 CO2
B. KClO3 t0 KCl + O2 D . Cả A,B,C đều đúng
Câu 12: Hòa tan hoàn toàn 9.2g kim loại Na vào nước sẽ thu được khối lượng NaOH và có thể tích H2(đktc) lần lượt là:
A.16g và 4.48 l B.8g và 4.48 l
C.16g và 2.24 l D.5g và 11.2 l
Câu 13: Phản ứng oxi hóa – khử là phản ứng hóa học trong đó xảy ra đồng thời:
A.Chất khử và chất oxi hóa B.Sự khử và sự oxi hóa
C.Sự khử và chất oxi hóa D.Sự oxi hóa và chât khử
Câu 14: Ở nhiệt độ xác định, dung dịch chưa bão hòa là dung dịch có thể hòa tan thêm:
A.Chất tan B.Dung môi C.Dung dịch D.Cả 3 chất trên
Câu 15: Cho phản ứng hóa học: Fe +CuSO4àFeSO4 + Cu. Phản ứng trên thuộc loại:
A.Phản ứng thế B. Phản ứng trao đổi
C. Phản ứng hóa hợp D.Phản ứng phân hủy
Câu 16: Cho 40g SO3 vào150g nước để tạo thành axit H2SO4. Khối lượng axit tạo thành là:
A.190g B.49g C.98g D.100g
II. PhầnTự luận (6 điểm )
Câu 17. (1điểm )
Bằng phương pháp hóa học hãy nhận biết ba chất rắn màu trắng mất nhãn gồm: CaO, P2O5, NaCl
Câu 18 (3 điểm)
Cho sơ đồ phản ứng: HCl + CuO CuCl2 + H2O
Dùng 50ml dung dịch axit HCl 1M tác dụng vừa đủ với CuO
a. Viết PTHH
b. Tính khối lượng CuO đã tham gia p/ư
c. Tính nồng độ CM của dung dịch ( Thể tích không thay đổi sau khi phản ứng)
Câu 19. ( 2 điểm) Đốt cháy hoàn toàn 1,12l CH4. Tính thể tích oxi cần dùng và thể tích khí CO2 tạo thành (đktc).
ĐÁP ÁN VÀ THANG ĐIỂM
Phần trắc nghiệm (4 điểm) mỗi câu đúng 0,25 điểm
II.PhầnTự luận ( 6 điểm)
YOPOVN xin gửi đến quý thầy cô, các em Đề kiểm tra học kì 2 môn hóa lớp 8 NĂM 2022 CÓ MA TRẬN + ĐÁP ÁN RẤT HAY. Đây là bộ Đề kiểm tra học kì 2 môn hóa lớp 8, đề thi hóa 8 học kì 2 có đáp án...........
Tìm kiếm có liên quan
De thi học kì 2 môn Hóa lớp 8 có đáp an
Trắc nghiệm Hóa 8 học kì 2 có đáp an
De thi Hóa lớp 8 học kì 2 tự luận
Các dạng bài tập Hóa lớp 8 học kì 2
vi|đề thi hóa lớp 8 học kì 2 năm 2020
vi|đề thi hóa lớp 8 học kì 1 năm 2020
De kiểm tra Hóa 8 giữa học kì 2
De kiểm tra Hóa 8 học kì 2
Các đề thi Hóa 8 giữa học kì 1
Trắc nghiệm Hóa 8 học kì 2 có đáp an
De thi Hóa 8 học kì 2 trắc nghiệm
De thi Hóa 8 giữa học kì 2 có đáp án
Các dạng bài tập Hóa 8 học kì 2
De thi Hóa lớp 8 học kì 2
vi|đề thi hóa lớp 8 học kì 2 năm 2020
Tổng hợp kiến thức hóa 8 học kì 2
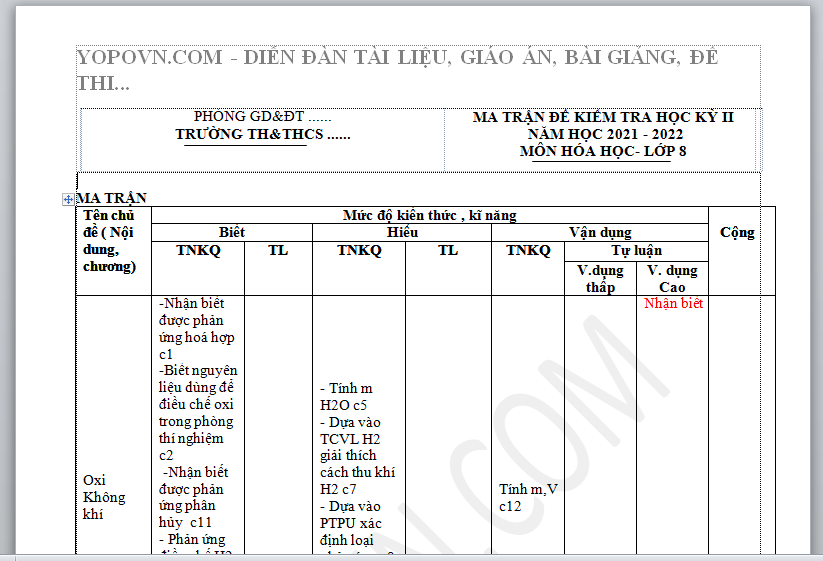
PHÒNG GD&ĐT ...... TRƯỜNG TH&THCS ...... | MA TRẬN ĐỀ KIỂM TRA HỌC KỲ II NĂM HỌC 2021 - 2022 MÔN HÓA HỌC- LỚP 8 |
MA TRẬN
| Tên chủ đề ( Nội dung, chương) | Mức độ kiến thức , kĩ năng | Cộng | ||||||
Biết | Hiểu | Vận dụng | ||||||
TNKQ | TL | TNKQ | TL | TNKQ | Tự luận | |||
V.dụng thấp | V. dụng Cao | |||||||
| Oxi Không khí | -Nhận biết được phản ứng hoá hợp c1 -Biết nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm c2 -Nhận biết được phản ứng phân hủy c11 - Phản ứng điều chế H2 trong công nghiệp c6 - Phân loại oxit c8 - Khái niệm PU oxi hóa – khử c13 | - Tính m H2O c5 - Dựa vào TCVL H2 giải thích cách thu khí H2 c7 - Dựa vào PTPU xác định loại phản ứng c9, c15 - Tính VO2 c10 | Tính m,V c12 | Nhận biết | ||||
| Số câu điểm % | 6 1,5 15 | 5 1,25 12,5 | 1 0,25 2,5 | | 1 1 10 | 13 4 40 | ||
Dung dịch | Tính được số gam chất tan có trong dung dịch c4 Khái niệm dd chưa bão hòa c14 | Tính được v chất phản ứng dựa theo phương trình hóa học | Tính Nồng độ của dung dịch c3 Tính mH20 c16 | Viết phương trình.Tính được khối lượng chất tham gia phản ứng. Tính Nồng độ của dung dịch | ||||
| Số câu điểm % | 2 0,5 5 | 1 2 20 | 2 0,5 5 | 1 3 30 | | 6 6 60 | ||
| Tổng | 8 câu 2 điểm 20 % | 1 câu 2 điểm 20 % | 7 câu 1,75điểm 17,5% | 1 câu 3 điểm 30 % | 1 câu 0,25điểm 2,5 % | 1 câu 1 điểm 10% | 19 câu 10 điểm 100% |
PHÒNG GD&ĐT ...... TRƯỜNG TH&THCS ...... | ĐỀ KIỂM TRA HỌC KỲ II NĂM HỌC 2021 - 2022 MÔN HÓA HỌC- LỚP 8 |
Hãy chọn một đáp án đúng nhất trong các câu (A, B, C, D) dưới đây
Câu 1: Phản ứng nào thuộc loại phản ứng hoá hợp :
A. CaCO3 + CO2 + H2O Ca(HCO3)2 C. C + O2 t0 CO2
B. KClO3 t0 KCl + O2 D . Cả A và C đúng
Câu 2. Nguyên liệu để điều chế oxi trong phòng thí nghiệm là :
A. KClO3 B. Không khí C. KMnO4 D. Cả Avà C đúng
Câu 3
A. 6% B. 25% C. 22 % D. 50%
Câu 4:Nồng độ phần trăm của dung dịch cho ta biết số gam chất tan có trong bao nhiêu gam dung dịch.
A. 100 B. 80 C. 150 D. 90
Câu 5 : Số gam nước thu được khi cho 4.2 lít H2 tác dụng với 1.4 lit khí oxi(các khí ở đktc) là:
A.3g B.2.25g C.3.375g D.4g
Câu 6 : Phản ứng hóa học có thể dùng điều chế H2 trong công nghiệp là:
A.2H2Oà2H2+O2 B.Fe+2HClàFeCl2+H2
C.Zn+2HClàFe2Cl2+H2 D.2Al+6HClà2AlCl3+H2
Câu 7: Khi thu khí H2 vào ống nghiệm bằng cách đẩy không khí, phải để úp ống nghiệm vì khí H2
A.Tan ít trong nước B.Nặng hơn không khí
C.Nhẹ hơn không khí D.Nhiệt độ hóa lỏng thấp nhật
Câu 8 : Cho biết công thức hóa học của các oxit sau: SO3, CO2, P2O5, Fe2O3, CaO.
A. Cả 5 oxit trên đều là oxit axit B.Cả 5 oxit trên đều là oxit bazzo
C.Cả 5 oxit trên đều là oxit trung tính D.5 oxit trên có cả oxit axit và oxit bazơ
Câu 9 : Cho phản ứng hóa học: 3H2 + Fe2O3 à 2Fe + 3H2O. phản ứng trên thuộc loại :
A .Phản ứng trao đổi B. Phản ứng oxi hóa – khử
C. Phản ứng hóa hợp D.Phản ứng phân hủy
Câu 10: Phân hủy hết 24,5 g KClO3 thu được thể tích O2 (đktc) là:
A.4.48 lt B.6.72 l C.22.4 l D.11.2 l
Câu 11: Phản ứng nào thuộc loại phản ứng phân hủy:
A. CaCO3 + CO2 + H2O Ca(HCO3)2 C. C + O2 t0 CO2
B. KClO3 t0 KCl + O2 D . Cả A,B,C đều đúng
Câu 12: Hòa tan hoàn toàn 9.2g kim loại Na vào nước sẽ thu được khối lượng NaOH và có thể tích H2(đktc) lần lượt là:
A.16g và 4.48 l B.8g và 4.48 l
C.16g và 2.24 l D.5g và 11.2 l
Câu 13: Phản ứng oxi hóa – khử là phản ứng hóa học trong đó xảy ra đồng thời:
A.Chất khử và chất oxi hóa B.Sự khử và sự oxi hóa
C.Sự khử và chất oxi hóa D.Sự oxi hóa và chât khử
Câu 14: Ở nhiệt độ xác định, dung dịch chưa bão hòa là dung dịch có thể hòa tan thêm:
A.Chất tan B.Dung môi C.Dung dịch D.Cả 3 chất trên
Câu 15: Cho phản ứng hóa học: Fe +CuSO4àFeSO4 + Cu. Phản ứng trên thuộc loại:
A.Phản ứng thế B. Phản ứng trao đổi
C. Phản ứng hóa hợp D.Phản ứng phân hủy
Câu 16: Cho 40g SO3 vào150g nước để tạo thành axit H2SO4. Khối lượng axit tạo thành là:
A.190g B.49g C.98g D.100g
II. PhầnTự luận (6 điểm )
Câu 17. (1điểm )
Bằng phương pháp hóa học hãy nhận biết ba chất rắn màu trắng mất nhãn gồm: CaO, P2O5, NaCl
Câu 18 (3 điểm)
Cho sơ đồ phản ứng: HCl + CuO CuCl2 + H2O
Dùng 50ml dung dịch axit HCl 1M tác dụng vừa đủ với CuO
a. Viết PTHH
b. Tính khối lượng CuO đã tham gia p/ư
c. Tính nồng độ CM của dung dịch ( Thể tích không thay đổi sau khi phản ứng)
Câu 19. ( 2 điểm) Đốt cháy hoàn toàn 1,12l CH4. Tính thể tích oxi cần dùng và thể tích khí CO2 tạo thành (đktc).
Theo sơ đồ phản ứng: CH4 + O2 CO2 + H2O
PHÒNG GD&ĐT ...... TRƯỜNG TH&THCS ...... | HƯỚNG DẪN CHẤM KIỂM TRA HỌC KỲ II NĂM HỌC 2021 - 2022 MÔN HÓA HỌC- LỚP 8 |
ĐÁP ÁN VÀ THANG ĐIỂM
Phần trắc nghiệm (4 điểm) mỗi câu đúng 0,25 điểm
Câu 1 | Câu 2 | Câu 3 | Câu 4 | Câu 5 | Câu 6 | Câu 7 | Câu 8 |
D | D | B | A | B | A | C | D |
Câu 9 | Câu 10 | Câu 11 | Câu 12 | Câu 13 | Câu 14 | Câu 15 | Câu 16 |
B | B | B | A | B | A | A | B |
II.PhầnTự luận ( 6 điểm)
| 17 | - Lấy mỗi dung dịch một ít cho vào nước và thử bằng quỳ tím - Dung dịch làm quỳ tím chuyển màu đỏ là H3PO4 - Dung dịch làm quỳ tím chuyển màu xanh là Ca(OH)2 - Dung dịch còn lại là NaCl | 0,5 0,5 |
| 18 | nHCl =0,05. 1=0,05 (mol) 2HCl +CuO CuCl2 +H2O 2mol 1mol 1mol nCuO = nCuCl2=1/2 nHCl mCuO=0,025 . 80 =2 (gam) cM CuCl2 ==0,5( mol) | 0,5 0,5 0,5 0,5 0,5 0,5 |
19 | a. b. CH4 + 2O2 CO2 + 2H2O | 0,5 0,5 0,5 0,5 |




